1. Eine zu große Menge an Säuren schädigt die Knochen
![]() Kochsalz enthält beides: mit Natrium eine starke Base und mit Chlorid einen starken Säurebildner (z. B. als Bestandteil der Salzsäure). Man könnte daher davon ausgehen, dass Kochsalz in der Gesamtbilanz auch neutral verstoffwechselt wird.
Kochsalz enthält beides: mit Natrium eine starke Base und mit Chlorid einen starken Säurebildner (z. B. als Bestandteil der Salzsäure). Man könnte daher davon ausgehen, dass Kochsalz in der Gesamtbilanz auch neutral verstoffwechselt wird.
____
** 1 g NaCl ≙ 17 mmol Na ≙ 0,4 g Na
Eine ständige, hohe Kochsalzzufuhr führt zu einer schwachen, auf Dauer aber problematischen Übersäuerung des Blutes (metabolische Azidose). Besondere Beachtung verdient diese Verschiebung wegen der erhöhten Knochenabbaurate (Osteoporose), die sie bewirkt.
Michael Martin, Autor des Buches Labormedizin in der Naturheilkunde, schreibt:
 „Die Homöostase zur Aufrechterhaltung eines physiologischen pH-Milieus funktioniert bei ungünstiger Lebensweise bzw. bei unerkannter milder Azidose nur auf Kosten des Knochenmineralgehaltes, da eine metabolische Azidose die Freisetzung von Kalzium aus dem Knochen bewirkt, um die überschüssigen Protonen zu puffern.“[103. Michael Martin, „Osteoporose, Anti-Aging und der Säure-Basenhaushalt“, „Internet: http://www.freieheilpraktiker.com/Patienteninfo/Naturheilkunde/Osteoporose-Anti-Aging-und-der-Saeure-Basenhaushalt (Stand 02.2011).]
„Die Homöostase zur Aufrechterhaltung eines physiologischen pH-Milieus funktioniert bei ungünstiger Lebensweise bzw. bei unerkannter milder Azidose nur auf Kosten des Knochenmineralgehaltes, da eine metabolische Azidose die Freisetzung von Kalzium aus dem Knochen bewirkt, um die überschüssigen Protonen zu puffern.“[103. Michael Martin, „Osteoporose, Anti-Aging und der Säure-Basenhaushalt“, „Internet: http://www.freieheilpraktiker.com/Patienteninfo/Naturheilkunde/Osteoporose-Anti-Aging-und-der-Saeure-Basenhaushalt (Stand 02.2011).]
Dass zuviel Kochsalz die Knochen entkalkt, ist durch viele Studien belegt. [104. Velimir Matkovic et al., „Urinary calcium, sodium, and bone mass of young females“, Am. J. of Clin. Nutr. 1995;62:417-425. Internet: http://www.mineralmed.com.pt/documentos/pdf/aae2dd3b-f5e6-4092-972e-fa37359e31e6.pdf (Stand: 10.2014). / Amanda Devine et al., „A longitudinal study of the effect of sodium and calcium intakes on regional bone density in postmenopausal women“, Am. J. of Clin. Nutr. 1995;62:740-745. Internet: http://ajcn.nutrition.org/content/62/4/740.full.pdf (Stand: 10.2014). / Robert P. Heaney, „Role of Dietary Sodium in Osteoporosis“, Journal of the American College of Nutrition, Vol. 25, No. 90003, 271S-276S (2006). Internet: http://www.tandfonline.com/doi/abs/10.1080/07315724.2006.10719577#.VDu801d6MqE (Stand: 10.2014).]Erhöhen wir die tägliche Natriumzufuhr um 100 mmol ( ≙ 5,9 g Kochsalz)**, führt dies zu einer um 0,5 bis 1,5 mmol erhöhten Calciumausscheidung (Heaney 2006). Ein nicht kompensierter Calciumverlust von 1 mmol täglich hat wiederum zur Folge, dass dem Skelett jährlich 1 % Calcium entzogen wird (Goulding 1990). Auch wenn diese Entmineralisierung schleichend verläuft, kann sie letztendlich doch zu Osteoporose führen.
Die folgenden Grafiken basieren auf den Daten der Dissertation von Dr. Petra Frings-Meuthen.[105. Petra Frings-Meuthen, „Einfluss einer hohen Kochsalzzufuhr auf die Natriumspeicherung, den Knochenstoffwechsel und den Säure-Basen Haushalt bei ambulanten sowie immobilisierten Probanden“, Dissertation (2008) am Institut für Ernährungs- und Lebensmittelwissenschaften. Internet: http://hss.ulb.uni-bonn.de/2009/1663/1663.pdf (Stand: 10.2014).] Sie zeigen die kurzfristigen Auswirkungen einer hohen Kochsalzzufuhr auf den Blut-pH-Wert und den Knochenstoffwechsel. Die Probanden waren gesund, männlich und zwischen 20 und 35 Jahre alt.
Die Studie dauerte 28 Tage und war in 4 Phasen unterteilt:
- 1.-6. Tag: Kochsalzzufuhr ca. 2,9 g/Tag
- 7.-12. Tag: Kochsalzzufuhr ca. 11,5 g/Tag
- 13.-22. Tag: Kochsalzzufuhr ca. 31,6 g/Tag
- 23.-28. Tag: Kochsalzzufuhr ca. 2,9 g/Tag
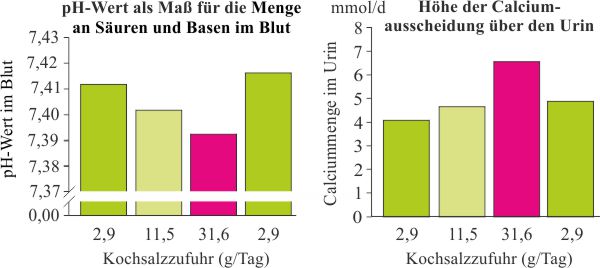
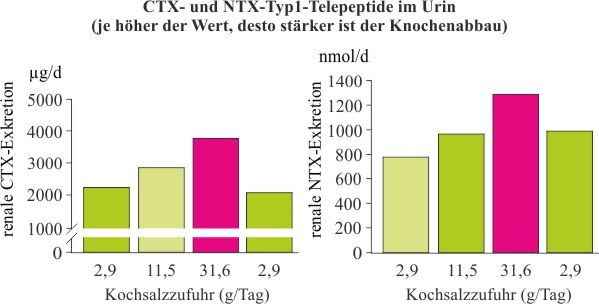
Dr. Frings-Meuthen schreibt:
 „Die Erzeugung einer milden metabolischen Azidose, als Folge einer hohen Kochsalzzufuhr, stellt einen potentiellen Mechanismus der kochsalzbedingten erhöhten Knochenresorption dar und eröffnet somit ein neues Feld an potentiellen Gegenmaßnahmen.“
„Die Erzeugung einer milden metabolischen Azidose, als Folge einer hohen Kochsalzzufuhr, stellt einen potentiellen Mechanismus der kochsalzbedingten erhöhten Knochenresorption dar und eröffnet somit ein neues Feld an potentiellen Gegenmaßnahmen.“
Als „logische“ Konsequenz empfehlen die meisten Mediziner calciumreiche Lebensmittel. Inzwischen ist aber durch zahlreiche Studien abgesichert, dass das allein nichts bringt. Betrachtet man die Struktur der Knochen genauer, so erkennt man, dass sie aus einem Verbund von eiweißhaltigem Bindegewebe (Kollagen) bestehen, das für die Elastizität sorgt, und Calcium, Phosphor und Magnesium, die für die Festigkeit wichtig sind. Wichtige Co-Faktoren, die den Einbau von Calcium überhaupt erst ermöglichen, sind eiweißhaltige Enzyme, Vitamin D, Magnesium, Kieselsäure (Silizium), Zink – und natürlich Bewegung (Druck- und Zugbelastung).
Damit Calcium nicht nutzlos ausgeschieden wird, benötigen wir Magensäure. Wer davon genügend hat, dem genügt in der Regel die tägliche Calciumaufnahme mit natürlichen Lebensmitteln. Eine zusätzliche Zufuhr durch Nahrungsergänzungsmittel kann sich sogar negativ auswirken, da sich dadurch das Schlaganfall- und Herzinfarktrisiko erhöhen.[106. Philipp Grätzel von Grätz, „Wieviel Kalzium bei Osteoporose?“, ÄrzteZeitung, 29.04.2009, Internet: http://www.aerztezeitung.de/medizin/krankheiten/herzkreislauf/herzinfarkt/article/544471/wieviel-kalzium-osteoporose.html (Stand: 10.2014).]
Anders verhält es sich bei Menschen, die Säureblocker zu sich nehmen, denn hierdurch wird die Calciumverwertung stark beeinträchtigt.
Für solche Menschen sind die gängigen Calciumkarbonat-Produkte, die man in jedem Supermarkt in Form von Brausetabletten erhält, allerdings wertlos. Sie benötigen Calciumgluconat oder Calciumcitrat, die sich auch ohne Säure im Verdauungssystem auflösen. Wer zu wenig Magensäure hat, schwächt seine Knochen auch auf andere Weise, da bei ihm die Effektivität der Eiweißsynthese eingeschränkt ist.
Wie Prof. Robert P. Heaney von der Creighton University (Omaha, USA) nachweisen konnte, ist eine höhere Kaliumzufuhr wiederum das beste Mittel, um kochsalzbedingten Knochenschäden entgegenzuwirken. Kaliumverbindungen, wie das in Obst oder Gemüse enthaltene Kaliummalat und Kaliumcitrat, werden im Organismus zu Kaliumbicarbonat umgewandelt.
Damit ist die Knochenzelle in der Lage,
- den Säureüberschuss zu neutralisieren (nicht nur den, der durch Kochsalz entsteht) und
- die erhöhte Calciumausscheidung zu stoppen.
Weitere positive Auswirkung: eine höhere Knochendichte, und durch die geringere Ausscheidung von Calcium auch weniger calciumbedingte Harn- und Nierensteine.
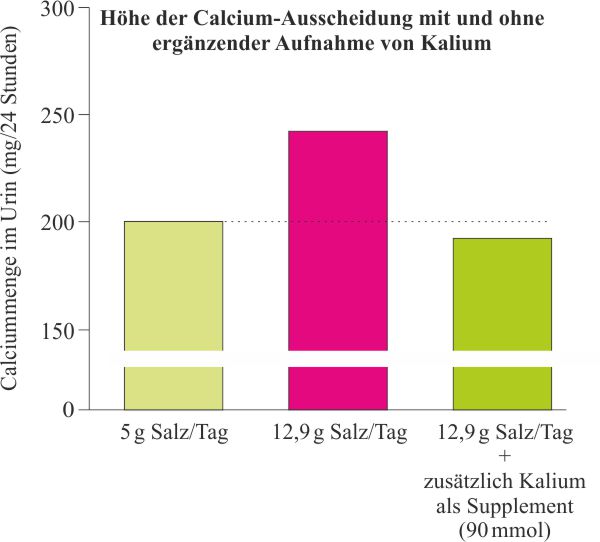
Quelle : nach Robert P. Heaney, „Role of Dietary Sodium in Osteoporosis“,
Journal of the American College of Nutrition, Vol. 25, No. 90003, 271S-276S (2006)
Nach dieser Untersuchung ist Kalium nicht nur in der Lage, den übermäßigen Calciumverlust abzumildern. Es senkt ihn trotz einer hohen täglichen Salzmenge sogar unter den Wert der relativ moderaten Salzzufuhr.
3. Die Bedeutung von Magnesium
Betrachtet man Magnesium aus der Warte des Knochenstoffwechsels, erfüllt es drei wichtige Aufgaben:
- Wie Calcium ist Magnesium ein strukturbildendes Mineral.
- 50-55 % des Körpermagnesiums befindet sich als Langzeitdepot in den Knochen. Dadurch kann man einen latenten Magnesiummangel im Blut bzw. in den Zellen ausgleichen.
- Magnesium aktiviert viele biochemische Reaktionen für den Knochenaufbau und erhalt.
- Als Bestandteil des Enzyms „alkalische Phosphatase“, wird es zur Bildung Hydroxylapatit benötigt[107. Deutsche Gesellschaft für Nährstoffmedizin und Prävention e. V. (DGNP), „Magnesium“, http://www.vitalstoff-lexikon.de/Mineralstoffe/Magnesium (Stand: 10.1014).] (ein wichtiger Grundbaustein beim Aufbau von Knochengewebe).
- Durch die Stimulierung der PTH*-Sekretion aus der Nebenschilddrüse ist Magnesium an der Regulation des Plasma-Calcium-Spiegels beteiligt.[108. Robert K. Rude, „Magnesium Deficiency: A Cause of Heterogenous Disease in Humans“, J Bone Miner Res. 1998 Apr;13(4):749-758. Internet: http://onlinelibrary.wiley.com/doi/10.1359/jbmr.1998.13.4.749/full (Stand: 10.2014).]
- Magnesium fördert auch die Umwandlung von Vitamin D3 in das aktive Hormon 1,25-Dehydroxy-Cholecalciferol. [109. Robert K. Rude, John S. Adams, Elisabeth Ryzen, David B. Endres, Hiroo Niimi, Ronald L. Horst et al., „Low serum concentrations of 1,25-dihydroxyvitamin D in human magnesium deficiency“, J Clin Endocrinol Metab. 1985 Nov;61(5):933-940. Internet: http://press.endocrine.org/doi/abs/10.1210/jcem-61-5-933 (Stand: 10.2014).]Vitamin D spielt eine wesentliche Rolle bei der Calciumaufnahme aus dem Darm, der Regulierung des Calcium-Spiegels im Blut und der Mineralieneinlagerung zum Aufbau der Knochen.
- Als Co-Faktor für die Herstellung von ATP ist Magnesium als Energiegeber für die Knochenmineralisation unverzichtbar.
* Parathormon, Parathyrin
Studien
L. Cohen und R. Kitzes untersuchten nach einer Beckenkammbiopsie das entnommene Gewebe. Von 19 postmenopausalen Frauen, die alle an Osteoprose erkrankt waren, hatten 16 einen erniedrigten Magnesiumgehalt im Knocheninnern (trabekulärer Knochenanteil).[110. L. Cohen, R. Kitzes, „Infrared spectroscopy and magnesium content of bone mineral in osteoporotic women“, Isr J Med Sci. 1981 Dec;17(12):1123-1125. Internet: http://www.ncbi.nlm.nih.gov/pubmed/7327911 (Stand: 10.2014).]
Das Ergebnis einer Studie der University of Southern California und des Orthopaedic Hospital in Los Angeles war: langsamere Mineralisierung von Knorpel- und Knochengewebe bei Magnesiummangel.[111. Robert K. Rude, Helen E. Gruber, „Magnesium deficiency and osteoporosis: animal and human oberservations“, J Nutr Biochem. 2004 Dec;15(12):710-716. Internet: http://www.sciencedirect.com/science/article/pii/S0955286304001573 (Stand: 10.2014).]
Die Tufts University in Boston (USA) stellte fest, dass sowohl ein hoher Kalium- wie auch ein hoher Magnesiumanteil in der Ernährung eine erheblichen Rolle beim Erhalt der Knochendichte älterer Menschen spielt.[112. Katherine L. Tucker et al., „Potassium, magnesium, and fruit and vegetable intakes are associated with greater bone mineral density in elderly men and women“, American Journal of Clinical Nutrition Vol. 69, No. 4, 727-736, April 1999. Internet: http://ajcn.nutrition.org/content/69/4/727.full.pdf (Stand: 10.2014).]
Forscher an der University of Tennessee (USA) untersuchten die Knochendichte (BMD – bone mineral density) von 2038 Männern und Frauen im Alter von 70 bis 79 Jahren. Um andere Faktoren bereinigt (Alter, Rasse, Body Mass Index, Rauchen, Alkoholkonsum, körperliche Aktivität, Östrogentherapie, Nahrungsergänzungen in Form von Calcium und Vitamin D), ergab sich Folgendes: Weiße Frauen mit der höchsten Magnesium-Aufnahme hatten im Vergleich zu Frauen mit einer geringen Magnesiumzufuhr eine um 0,04 g/cm2 höhere Knochendichte. Bei den Männern war sie um 0,02 g/cm2 höher.
Wie eine Gruppe von Wissenschaftlern um Thomas O. Carpenter von der Yale University School of Medicine (New Haven, USA) nachweisen konnte, lässt sich durch Magnesium auch die Knochendichte von Kindern und Jugendlichen erhöhen.[113. Thomas O. Carpenter et al., „A randomized controlled study of effects of dietary magnesium oxide supplementation on bone mineral content in healthy girls“, J Clin Endocrinol Metab. 2006 December; 91(12): 4866-4872. Internet: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2995550/ (Stand: 10.2014).] An der placebo-kontrollierten, randomisierten Doppelblindstudie nahmen 122 gesunde Mädchen im Alter zwischen 8 bis 14 Jahren teil. Davon wurden 50 ausgewählt, deren ernährungsbedingte Magnesium-Aufnahme weniger als 220 mg/Tag betrug. Aufgeteilt in zwei Gruppen, erhielten sie über einen Zeitraum von 12 Monaten entweder 300 mg Magnesium täglich oder ein Placebo. Gegenüber den Mädchen, die ein Placebo erhielten, war der Mineralgehalt der Knochensubstanz (BMC) in der Magnesium-Gruppe im Hüftbereich signifikant und in der Lendenwirbelsäule leicht höher.
Prof. Dr. med. Diethard M. Usinger bringt die positive Wirkung von Magnesium in dem Buch Osteoporose: Ein Ratgeber für Betroffene, Angehörige und medizinisches Fachpersonal auf den Punkt:
 „Es fördert die Aktivität der knochenaufbauenden Zellen (Osteoblasten), aktiviert das Vitamin D, erleichtert den Kalziumtransport und erhöht die Mineraliendichte im Knochen. Es verbessert die Reaktion des Knochens auf das Parathormon und auf das Vitamin D.“[114. Diethard M. Usinger, Osteoporose: Ein Ratgeber für Betroffene, Angehörige und medizinisches Fachpersonal, Schulz-Kirchner (2007), S. 57.]
„Es fördert die Aktivität der knochenaufbauenden Zellen (Osteoblasten), aktiviert das Vitamin D, erleichtert den Kalziumtransport und erhöht die Mineraliendichte im Knochen. Es verbessert die Reaktion des Knochens auf das Parathormon und auf das Vitamin D.“[114. Diethard M. Usinger, Osteoporose: Ein Ratgeber für Betroffene, Angehörige und medizinisches Fachpersonal, Schulz-Kirchner (2007), S. 57.]
Betrachtet man sämtliche Stoffwechselbedürfnisse, benötigt man
- Proteinlieferanten*, Calcium, Phosphat und Magnesium als Knochenbestandteile,
- Enzyme, Magnesium, Silizium, Zink, Kupfer, Mangan, die Vitamine B6 und B12, C, D, E und K, ausreichend Magensäure sowie Bewegung, um den Knochenaufbau zu fördern,
- Kalium und andere basische Mineralien, um einer Knochenentkalkung vorzubeugen,
- Magnesium, um zu verhindern, dass sich zu viele Calcium-Ionen mit der Oxalsäure zu Calcium-Oxalat verbinden.
Mehr Natrium → höhere Urin-Calcium-Ausscheidung
Calcium ist bei weitem nicht nur ein strukturgebendes Mineral zum Aufbau von Knochen und Bindegewebsfasern. Auch grundlegende Stoffwechselvorgänge wie Nerven- und Muskelaktivität, bestimmte hormonelle und enzymatische Regulationsabläufe, Blutgerinnung, Wundheilung oder die Narbenbildung sind von einer ausreichenden Calciumversorgung abhängig.
Im Zusammenhang mit der Zellmembran und der Natrium-Kalium-Pumpe steuert es verschiedene Transportprozesse, oder genauer gesagt die Ionenströme. Man kann sich die Zellmembran wie ein Sieb vorstellen, das innerhalb von Millisekunden seine Löcher schließt oder öffnet. Der Fachausdruck hierfür ist selektive Permeabilität – und hieran ist Calcium beteiligt, indem es die Durchlässigkeit der Ionen-Kanälchen für Kalium und Natrium beeinflusst. Das beeinflusst nicht nur die Natrium-Kalium-Pumpe, sondern auch den Wasserhaushalt und das Ruhe- und Aktionspotential der Nerven- und Muskelzellen (einschließlich der Gefäß- und Herzmuskelzellen). Des Weiteren „dichtet“ Calcium die Zellmembran gegen eine zu hohe Histaminausschüttung ab, sodass die Intensität von allergischen und juckreizauslösenden Reaktionen gemindert wird.
Störungen des Calcium-Haushalts begünstigen daher eine Vielzahl von Krankheiten. Der Einfluss von Kochsalz ergibt sich nicht nur aus der Säurebelastung, sondern auch dadurch, dass sowohl Calcium wie auch Natrium das gleiche Transportsystem im proximalen Tubulus (dem Hauptstück der Nierenkanälchen) nutzen.
 Nach Prof. Connie M. Weaver vom Foods & Nutrition der US-amerikanischen Universität Purdune ist von den Ernährungsfaktoren, die zu Urin-Calcium-Verlusten führen (Protein, Koffein und Natriumzufuhr), Natrium der wichtigste.
Nach Prof. Connie M. Weaver vom Foods & Nutrition der US-amerikanischen Universität Purdune ist von den Ernährungsfaktoren, die zu Urin-Calcium-Verlusten führen (Protein, Koffein und Natriumzufuhr), Natrium der wichtigste.
Pro Gramm Natrium, das die Niere ausscheidet, werden auch 17 bis 26 Milligramm Calcium ausgeschieden. Ein weiterer Punkt, den Weaver zu bedenken gibt: Eine Verdopplung der Proteinzufuhr führt zu einem 50%-igen Anstieg der Urin-Calcium-Ausscheidung. Wer dagegen viel Kalium mit der Ernährung zuführt, reduziert auch bei einer Ernährung mit hohem Proteinanteil den Urin-Calcium-Verlust.[115. Roland L. Weinsier, Carlos L. Krumdieck (2000), „Dairy foods and bone health: examination of the evidence“, American Journal of Clinical Nutrition, 72, 681-689. Internet: http://ajcn.nutrition.org/content/72/3/681.short (Stand: 10.2014).] Gleichzeitig trägt das zur Erhaltung der Knochendichte bei.
Käse, der in der Regel natriumreich, eiweißreich und kaliumarm ist, trägt deshalb kaum zur Calciumversorgung bei. Bei Wurst und gewürzten Fertigfleischprodukten ist die Bilanz sogar negativ.
Copyright, Layout, Text, Grafik: Claus Barta
Alle Rechte der Verbreitung, der Übersetzung und der Vervielfältigung vorbehalten. Dies gilt auch für Fotokopie, Internet, Tonträger oder in einer anderen Form. Auszugsweise Nachdrucke sind nur mit schriftlicher Genehmigung gestattet.
